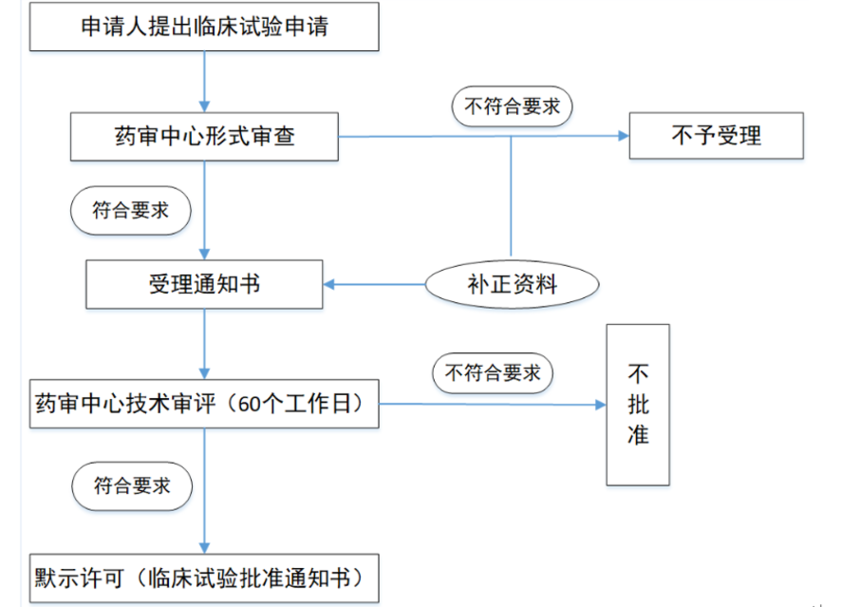
1. 申请人完成支持药物临床试验的药学、药理毒理学等研究后,向国家药品监督管理局药品审评中心(CDE)提出药物临床试验申请,按照申报资料要求提交相关研究资料。
2. 药品审评中心对申报资料进行形式审查,符合要求的,出具受理通知书;不符合要求的,出具不予受理通知书或者申请材料补正通知书,并说明理由。
3. 药品审评中心组织药学、医学和其他技术人员对已受理的药物临床试验申请进行审评,自受理之日起60个工作日内决定是否同意开展药物临床试验,并通过CDE网站通知申请人审批结果;逾期未通知的,视为同意,申请人可以按照提交的方案开展药物临床试验。
1. 申请人在完成支持药品上市注册的药学、药理毒理学和药物临床试验等研究,确定质量标准,完成商业规模生产工艺验证,并做好接受药品注册核查检验的准备后,向药品审评中心提出药品上市许可申请,按照申报资料要求提交相关研究资料。
2. 药品审评中心对申报资料进行形式审查,符合要求的,出具受理通知书;不符合要求的,出具不予受理通知书或者申请材料补正通知书,并说明理由。
3. 药品审评中心组织药学、医学和其他技术人员,在规定时限内对已受理的药品上市许可申请进行审评。
4. 审评过程中基于风险启动药品注册核查、检验,相关技术机构应当在规定时限内完成核查、检验工作。
5. 药品审评中心根据药品注册申报资料、核查结果、检验结果等,对药品的安全性、有效性和质量可控性等进行审查,综合审评结论通过的,批准药品上市,发给药品注册证书。不予批准,发给《药品上市许可不予批准通知书》。














