|
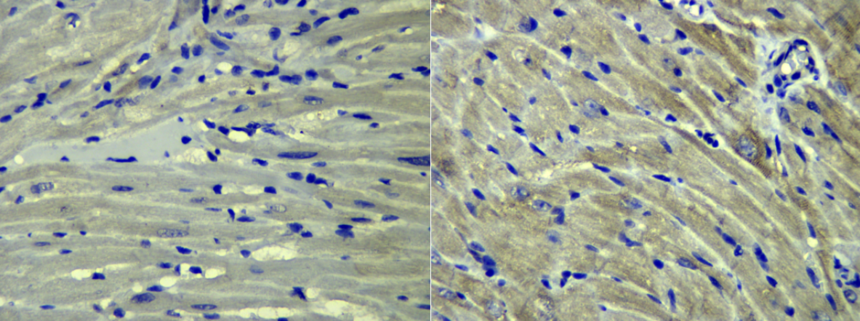
全胚胎免疫组织化学染色细胞质内弥散性分布,多数免疫组织化学染色为胞质型阳性反应,如细胞角蛋白(Cytokeratin,CK)和波形蛋白(Vimentin)等。 细胞核周边胞质内分布,其判别要点是细胞核轮廓被勾画得很清楚,如CD3多克隆抗体的染色。 胞浆内局限性点状阳性反应,如CDI$抗体的染色。 细胞膜线性阳性反应,大多数淋巴细胞标志物的染色均如此,如CD20。 细胞核阳性反应,如BrdU、Ki-67及雌、孕激素受体蛋白等。 有些抗原的阳性表达可同时出现在细胞的不同部位,如细胞质和细胞膜等。
计算免疫反应阳性细胞数方法是选择每个样品中10个非重叠视野,计算每个视野中的阳性细胞与总细胞数的百分比,取平均数,连续观察和计算至少二个条件相同的样品。得出数据经统计学处理后可在计算机Microsoft Excel中作出柱形图。 另一种方法以染色阳性强度和阳性检出率相结合而定,一般阳性细胞数在0~25为阴性,25~50为+,50~75为++,75以上为+++。此种判定方法容易出现人为误差,现已很少在论文中出现。 图像分析系统检测阳性结果。 针对以上的评判标准,常规免疫组织化学染色在有些时候是不能满足我们对实验的要求,这个时候就可能会用到一些非常规的免疫组织化学染色方法,比如全组织免疫组织化学染色,全组织免疫组织化学染色尤其是胚胎,是指组织并没有切片,而是组织的一小块进行的整体染色方法。胚胎干细胞、胚胎发育学研究者以及神经学者通过动物的不同发育阶段表达不同的目的蛋白这一特点而对不同阶段的动物全胚胎进行染色。 全组织染色与免疫细胞化学以及冰冻切片染色十分类似。如果一种抗体可以应用于冰冻切片(并不包括石蜡包埋的切片)染色中的话,那么在全胚胎染色中也是适用的。不同之处在于全胚胎染色的样品比正常的切片样品更大更厚。因此,固定、封闭、抗体孵育、洗脱、通透以及底物显色过程都需要更长的时间,以使得溶液可以渗透到达样品的中心。虽然研究者们使用不一样的次数,但必要的话这些步骤中的细节对于优化实验也可以提供指导。 随着胚胎的生长,越大的胚胎越难染色。像固定液、抗体、显影液等试剂也不易于渗透到样品的中心,染色的细胞很难获得一个清晰的图像。那么,必要的话,大的或者后期的胚胎可以在染色之前可以将其分开成几块。 推荐年龄: (1)鸡胚胎:6天;(2)鼠胚胎:12天等 获取胚胎:列举常见几种。 鸡:轻柔的将一个鸡蛋打到一个干净的中等大小的玻璃培养皿中。胚胎一般漂浮在蛋黄的顶端。使用干净的剪刀和装有枪头的Pasteur移液管即可轻松的获取胚胎。(这样可以避免胚胎来自移液管窄尖头的损坏) 鼠:在成年雌鼠中取胚胎。在预冷的PBS中解剖胚胎,尽可能移去不需要的组织。我们建议尽可能多的去除胚胎膜和额外不需要的组织。这能够避免抗体散布到整个胚胎上。 果蝇:制备特殊琼脂培养基,等果蝇产卵之后,用软毛刷轻轻刷琼脂表面,使酵母泥和胚胎脱落到水里。将水倒入筛子里。重复两三次,使胚胎完全转移到筛子里。将筛子半浸入盛水的容器里用毛刷洗一下,然后在自来水(开小一点)下冲洗干净,用称量用的刮刀转移到EP管里。 将胚胎用4%多聚甲醛固定液浸泡,置于4℃固定。固定的时间需要优化。建议优化的时间间于2h和过夜之间。 或者用m-DMSO(80%甲醇,20%的DMSO)固定。 一般地,使用同一种抗体时,在冰冻切片中成功使用的固定液,一般都适合用来做全组织染色的。然而,这也是需要做一些优化的。 当样品完全浸透固定液时就会沉入溶液瓶底。注意在进行接下来的步骤时一定要确保样品沉入溶液底部。 用含0.5-1%trion的PBS清洗三次,每次30分钟。 用封闭液(含1%Triton、10%胎牛血清、0.2%叠氮化钠的PBS)室温孵育胚胎1h。 阻断过氧化物酶:将胚胎置于含0.1%H2O2的封闭液中4°C过夜。 用封闭液清洗胚胎2次。 将Pasteur移液管末端剪掉形成2ml的管子,用其转移胚胎。加入合适浓度的一抗。 一般在全胚胎染色中抗体孵育的时间比较久,为了防止微生物的生长,在稀释一抗的封闭液中会加入0.02%的叠氮化钠。 样品在混合器上4°C缓慢旋转孵育1-4天。根据不同的抗体以及胚胎的大小,孵育的时间需要进行一些优化。 用含1%Triton、10%胎牛血清和0.2%叠氮化钠的PBS清洗胚胎3次,每次1h。 用含1%Triton的PBS清洗3次,每次10分钟。为防止叠氮化钠的残留影响显影时过氧化物酶的活性,清洗过程要彻底。 二抗孵育:用不含叠氮化钠的封闭液稀释二抗。 样品在混合器上4°C缓慢旋转孵育2-4天。 用含1%Triton的PBS清洗3次,每次10分钟。 用DAB底物室温孵育胚胎2-3h。 将胚胎转移到一个碟子中,加入新鲜的配制的显示底物(每1mlDAB加5ul的过氧化氢)。 用PBS清洗3次,使得样品达到理想的染色强度。 爬片观察胚胎:观察分析前样品于4°C避光储存。 将样品放置于100%的甘油中48h。当样品完全浸透甘油时会沉入瓶子底部。在进行下一步操作前一定要确保样品完全浸透甘油。 明胶常用来爬片,将样品装置于玻片上。而75%的甘油的密度和明胶的密度接近,故样品在染色后要浸透在75%的甘油中约15分钟。当样品完全浸透甘油时会沉入瓶子底部。 将样品置于50%的甘油中直到完全沉入瓶底。胚胎这个时候就可以观察了,或者爬片后观察。在盖玻片周围滴加油脂保护。 如果样品包埋在明胶中切片的话,可将20%的明胶65°C预热,在样品爬片前,将其置于明胶中约30分钟,使其完全浸透。当样品完全浸透时,会沉入瓶子底部。 全胚胎组织免疫荧光染色实验结果展示:
5X解剖镜下的荧光乌龟胚胎,采用荧光染色法 |